Formy sněžení a sněhové rekordy
Sněhem rozumíme pevné skupenství vody, které je tvořeno specifickými ledovými krystaly seskupenými do sněhových vloček. Sněhové krystaly vznikají v přírodě při teplotě 0°C nebo nižší, z podchlazených vodních kapiček oblacích na krystalizačních jádrech nebo přímou desublimací vodní páry na krystalická jádra. Krystalizují v šesterečné krystalické soustavě a spojují se ve větší útvary - sněhové vločky a ty postupně rostou. Když sněhová vločka dosáhne dostatečné hmotnosti, začne padat k zemi. Tak se mění podmínky jejího růstu a padáním se růst vločky zrychluje. Dopadem vloček na zem a jejich ukládáním vzniká pórovitá vrstva bez pravidelného uspořádání jednotlivých krystalů, nazývaná sněhová pokrývka. Video zaznamenává sněhovou bouři na východě USA, kterou zachytil ve svém časosběrném snímku americký fotograf Mike Black. Ten 20 hodin trvající sněžení zrychlil 1800krát.
Proč je čisté sklo průhledné?
 Sklo bylo dříve známo jako obsidián, v přírodě se vyskytující vulkanická tavenina. K objevu skla došlo v Egyptě někdy kolem roku 3 000 př. n. l. Nejprve "skláři" nedokázali vyrobit čisté sklo a tak čisté průhledné sklo bylo po dlouhou dobu ceněnou zvláštností. Výroba skla se pak rozšířila ze Středního a Blízkého východu do Evropy, kde za časů Římské říše došlo k dalšímu rozvoji sklářství. Sklo patří mezi typické homogenní amorfní látky, neboť jeho struktura částic je na rozdíl od krystalických látek neuspořádaná. Částice jsou ve skle rozmístěny nepravidelně, hovoříme o krátkodosahovém uspořádání částic na malé vzdálenosti.Sklo se vyrábí ze skleněné taveniny roztavené ve sklářské peci. Tavenina je složena z oxidu křemičitého, který se získává z křemene nebo ze sklářského písku. Křemen má teplotu tání okolo 2 000 °C, proto se při výrobě přidávají alkalické látky (soda a potaš), které snižují teplotu tání na asi 1 000 °C. Odolnost skla vůči vodě se vylepšuje přidáním oxidu vápenatého. Jak je možné, že částice, ze kterých se sklo skládá umožňují světlo skrz něj projít?
Sklo bylo dříve známo jako obsidián, v přírodě se vyskytující vulkanická tavenina. K objevu skla došlo v Egyptě někdy kolem roku 3 000 př. n. l. Nejprve "skláři" nedokázali vyrobit čisté sklo a tak čisté průhledné sklo bylo po dlouhou dobu ceněnou zvláštností. Výroba skla se pak rozšířila ze Středního a Blízkého východu do Evropy, kde za časů Římské říše došlo k dalšímu rozvoji sklářství. Sklo patří mezi typické homogenní amorfní látky, neboť jeho struktura částic je na rozdíl od krystalických látek neuspořádaná. Částice jsou ve skle rozmístěny nepravidelně, hovoříme o krátkodosahovém uspořádání částic na malé vzdálenosti.Sklo se vyrábí ze skleněné taveniny roztavené ve sklářské peci. Tavenina je složena z oxidu křemičitého, který se získává z křemene nebo ze sklářského písku. Křemen má teplotu tání okolo 2 000 °C, proto se při výrobě přidávají alkalické látky (soda a potaš), které snižují teplotu tání na asi 1 000 °C. Odolnost skla vůči vodě se vylepšuje přidáním oxidu vápenatého. Jak je možné, že částice, ze kterých se sklo skládá umožňují světlo skrz něj projít?
Cínový mor
 S cínem se nejčastěji setkáváme v jeho bílé modifikaci, kdy za běžné teploty tvoří krystaly ve čtverečné soustavě. Snese i přechlazení na teploty hluboko pod bodem mrazu, ale za velmi tuhé zimy se samovolně může přeměnit rekrystalizací na šedou práškovou formu. Neznalost tohoto jevu byla údajně jednou z příčin neúspěchu Scottovy výpravy k jižnímu pólu v letech 1911-1912. Výprava s sebou vezla petrolej v nádobách spájených cínem. Ten se však ve velkých mrazech změnil v šedivý prášek, nádoby povolily a palivo z nich vyteklo. Ne nadarmo bývají šedé skvrny na povrchu bílého cínu označovány jako cínový mor.
S cínem se nejčastěji setkáváme v jeho bílé modifikaci, kdy za běžné teploty tvoří krystaly ve čtverečné soustavě. Snese i přechlazení na teploty hluboko pod bodem mrazu, ale za velmi tuhé zimy se samovolně může přeměnit rekrystalizací na šedou práškovou formu. Neznalost tohoto jevu byla údajně jednou z příčin neúspěchu Scottovy výpravy k jižnímu pólu v letech 1911-1912. Výprava s sebou vezla petrolej v nádobách spájených cínem. Ten se však ve velkých mrazech změnil v šedivý prášek, nádoby povolily a palivo z nich vyteklo. Ne nadarmo bývají šedé skvrny na povrchu bílého cínu označovány jako cínový mor.
Jak pijí kočky?
Zpomalené záznamy pití mléka kočkami z misky, dovedly vědce z amerických univerzit (Princetonu, Virginského polytechnického institutu a MIT) po tříletém zkoumání k překvapivému zjištění, že kočky využívají při pití zajímavým způsobem fyzikální zákony. Dosud se vědci domnívali, že kočky pijí z misky tekutinu podobně jako psi. Psi totiž ze svého jazyka vytvoří něco jako lžíci, kterou chlemtají tekutinu do tlamy. Kočky ale nenabírají tekutinu jazykem, využívají setrvačnosti pohybu tekutiny, kteou svým jazykem vyvolají. Svůj jazýček do mléka ponoří často jen nepatrně a tak jejich způsob pití vyžaduje dokonalou synchronizaci působení gravitační a setrvačné síly. Přesto pijí naprosto elegantně, efektivně a rychle.
Uhlíková forma tvrdší než diamant
 Uhlík se v přírodě vyskytuje ve dvou základních modifikacích - jako grafit a jako diamant. Během posledních let však byly laboratorně připraveny další modifikace. Zajímavé jsou sférické molekuly složené buď z pěti nebo šesti šestičlenných kruhů atomů uhlíku označované jako fullereny. Objev a studium této formy uhlíku přinesly v roce 1996 Nobelovu cenu Robertu F. Curlovi, Richardu E. Smalleymu a Haroldu W. Krotoovi. Z uhlíku pak začaly být uměle vyráběné nanotrubice. Jde o trubičky složené z atomů uhlíku o tloušťce pouhých několika nanometrů. A v neposlední řadě byl objeven nejpevnější materiál - grafen, který přinesl letos Nobelovu cenu Geimovi a Novoselovi. Tvoří jej rovinná síť vzájemně propojených atomů uhlíku uspořádaných do tvaru šestiúhelníků v jediné vrstvě. Jenomže vědci mají další představy o tom jak by mohly být ještě jinak uspořádány atomy uhlíku. Počítačovou simulací dokázali najít strukturu uhlíku, která je tvrdší než diamant.
Uhlík se v přírodě vyskytuje ve dvou základních modifikacích - jako grafit a jako diamant. Během posledních let však byly laboratorně připraveny další modifikace. Zajímavé jsou sférické molekuly složené buď z pěti nebo šesti šestičlenných kruhů atomů uhlíku označované jako fullereny. Objev a studium této formy uhlíku přinesly v roce 1996 Nobelovu cenu Robertu F. Curlovi, Richardu E. Smalleymu a Haroldu W. Krotoovi. Z uhlíku pak začaly být uměle vyráběné nanotrubice. Jde o trubičky složené z atomů uhlíku o tloušťce pouhých několika nanometrů. A v neposlední řadě byl objeven nejpevnější materiál - grafen, který přinesl letos Nobelovu cenu Geimovi a Novoselovi. Tvoří jej rovinná síť vzájemně propojených atomů uhlíku uspořádaných do tvaru šestiúhelníků v jediné vrstvě. Jenomže vědci mají další představy o tom jak by mohly být ještě jinak uspořádány atomy uhlíku. Počítačovou simulací dokázali najít strukturu uhlíku, která je tvrdší než diamant.
Proč jsou v hodinkách kameny?
 Pokud jste měli někdy rozdělané mechanické náramkové hodinky, tak jste si jistě povšimli při pohledu na strojek, červených kamínků. Jejich počet je u některých hodinek rovněž uváděn na ciferníku, popřípadě na spodním víčku pouzdra. Jde o rubín - růžový až červeně zbarvený drahokam sestávající převážně z minerálu korundu (Al2O3) s příměsí chrómu, způsobující jeho zbarvení. Proč se však rubíny v hodinkách používají?
Pokud jste měli někdy rozdělané mechanické náramkové hodinky, tak jste si jistě povšimli při pohledu na strojek, červených kamínků. Jejich počet je u některých hodinek rovněž uváděn na ciferníku, popřípadě na spodním víčku pouzdra. Jde o rubín - růžový až červeně zbarvený drahokam sestávající převážně z minerálu korundu (Al2O3) s příměsí chrómu, způsobující jeho zbarvení. Proč se však rubíny v hodinkách používají?
Jak vznikly tekuté krystaly
 Tekuté krystaly nás obklopují v předmětech každodenní potřeby - tvoří například displej kalkulačky, mobilního telefonu, fotoaparátu či obrazovky televize nebo monitoru počítače. Cesta k jejich objevu byla docela zvláštní a začala už v 19. století. Tehdy vědci objevili zvláštní materiál, když ponořili nervové vlákno do vody. Tato látka jevila ve světle zajímavé vlastnosti, proto se vědci snažili objevit i jiné podobné materiály.
Tekuté krystaly nás obklopují v předmětech každodenní potřeby - tvoří například displej kalkulačky, mobilního telefonu, fotoaparátu či obrazovky televize nebo monitoru počítače. Cesta k jejich objevu byla docela zvláštní a začala už v 19. století. Tehdy vědci objevili zvláštní materiál, když ponořili nervové vlákno do vody. Tato látka jevila ve světle zajímavé vlastnosti, proto se vědci snažili objevit i jiné podobné materiály.
Vlezlý petrolej
 Mezi kapaliny, které výborně smáčejí povrch všech těles, patří petrolej. Vyrábí se frakční destilací ropy při
Mezi kapaliny, které výborně smáčejí povrch všech těles, patří petrolej. Vyrábí se frakční destilací ropy při
Zkoušky tvrdosti
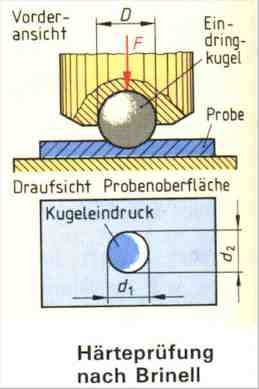 Tvrdostí rozumíme mechanickou vlastnost, která se používá především v technické praxi. Tvrdost je vlastně odpor materiálu proti pronikání jiného, tvrdšího materiálu. Tvrdé těleso se velmi nesnadno poškrábe. Primitivního, ale zato praktického způsobu, jak zjistit tvrdost nerostů, používají mineralogové. Sestavili posloupnost deseti nerostů podle toho, jak je možné jimi dělat vrypy do materiálu po nich následujících. Na vrcholu žebříčku je nejtvrdší přírodní materiál - diamant, který zanechává vryp na všech dalších nerostech. Jeho tvrdost se označuje číslem 10. Za ním následují korund, topaz, křemen, živec, apatit, fluorit (kazivec), kalcit (vápenec), kamenná sůl a nakonec mastek, který má stanovenu tvrdost 1. Tuto stupnici tvrdosti sestavil v roce 1822 Friedrich Mohs a nese tedy jeho jméno: Mohsova stupnice tvrdosti. Orientační tvrdost našeho nehtu se na této stupnici pohybuje kolem 2, u mincí až kolem 4, u kuchyňského nože asi 5.
Tvrdostí rozumíme mechanickou vlastnost, která se používá především v technické praxi. Tvrdost je vlastně odpor materiálu proti pronikání jiného, tvrdšího materiálu. Tvrdé těleso se velmi nesnadno poškrábe. Primitivního, ale zato praktického způsobu, jak zjistit tvrdost nerostů, používají mineralogové. Sestavili posloupnost deseti nerostů podle toho, jak je možné jimi dělat vrypy do materiálu po nich následujících. Na vrcholu žebříčku je nejtvrdší přírodní materiál - diamant, který zanechává vryp na všech dalších nerostech. Jeho tvrdost se označuje číslem 10. Za ním následují korund, topaz, křemen, živec, apatit, fluorit (kazivec), kalcit (vápenec), kamenná sůl a nakonec mastek, který má stanovenu tvrdost 1. Tuto stupnici tvrdosti sestavil v roce 1822 Friedrich Mohs a nese tedy jeho jméno: Mohsova stupnice tvrdosti. Orientační tvrdost našeho nehtu se na této stupnici pohybuje kolem 2, u mincí až kolem 4, u kuchyňského nože asi 5.
Kolik kapek vody se vejde na desetikorunu?
 S povrchovým napětím kapaliny je spojeno mnoho poměrně jednoduchých pokusů, ale o to se složitějším vysvětlením tohoto chování kapaliny. Při tomto jevu se povrch kapaliny chová jako tenká elastická blána či fólie. Ta se snaží zmenšit povrch kapaliny natolik, aby při určitém objemu kapaliny zaujal co nejmenší velikost. Kdyby na kapalinu nepůsobily další vnější síly, měla by ideální kulový tvar, neboť koule má ze všech těles stejného objemu nejmenší povrch. Vlivem působení například tíhové síly se však kulový tvar kapaliny deformuje. Tvar kulaté kapky tak mohou mít pouze malé kapičky rozlité rtuti nebo kapičky vodní mlhy. Kolik kapek vody se vám podaří nakapat například na desetikorunovou minci aniž by z jejího povrchu stekly dolů?
S povrchovým napětím kapaliny je spojeno mnoho poměrně jednoduchých pokusů, ale o to se složitějším vysvětlením tohoto chování kapaliny. Při tomto jevu se povrch kapaliny chová jako tenká elastická blána či fólie. Ta se snaží zmenšit povrch kapaliny natolik, aby při určitém objemu kapaliny zaujal co nejmenší velikost. Kdyby na kapalinu nepůsobily další vnější síly, měla by ideální kulový tvar, neboť koule má ze všech těles stejného objemu nejmenší povrch. Vlivem působení například tíhové síly se však kulový tvar kapaliny deformuje. Tvar kulaté kapky tak mohou mít pouze malé kapičky rozlité rtuti nebo kapičky vodní mlhy. Kolik kapek vody se vám podaří nakapat například na desetikorunovou minci aniž by z jejího povrchu stekly dolů?